据外媒报道,主要开发和推广治疗性大麻类新药的生物医药公司GW Pharmaceuticals及其子公司Greenwich Biosciences宣布,美国FDA的外周和中枢神经系统药物咨询委员会全票通过在研大麻二酚口服溶液(CBD,商品名Epidiolex®)的新药申请(NDA),用于辅助治疗两岁及以上患者的Lennox-Gastaut综合征(LGS)和Dravet综合征相关的癫痫发作。如果获批,Epidiolex将成为第一个基于CBD的药物制剂,也将是首个新型抗癫痫药物(AED)。预计今年6月27日FDA会完成对NDA的审查。
LGS和Dravet综合征通常在儿童期开始发展,是癫痫发作的严重破坏性形式。该病不仅对患者生命造成威胁,还加重了家庭和看护者肩上的担子。90%以上的LGS或Dravet综合征患者每天癫痫发作多次,很大可能会在此过程中跌倒和受伤。治疗LGS和Dravet综合征患者的医生努力使用目前可用疗法来减少危险癫痫发作的数量。如果Epidiolex获得批准,它将成为Dravet综合征患者的首个获批药物。
Epidiolex是GW的主要大麻素候选药物,是纯化CBD的药物制剂,用于治疗几种罕见的儿童期发作性癫痫症。截至目前,Epidiolex已获得FDA的孤儿药资格,用于治疗Dravet综合征、LGS、结节性硬化综合征(TSC)和婴儿痉挛(IS)。此外,该药物还获得FDA颁发的快速通道资格,用于治疗Dravet综合征。
此次GW展示的强大的临床开发项目包括三项随机对照的3期临床试验和一项开放标签扩展研究。在第3阶段的研究中,Epidiolex联合其他抗癫痫治疗,可显著降低LGS和Dravet综合征患者的癫痫发作频率。此外,Epidiolex通常耐受性良好,大多数不良事件报告为轻度或中度并且可控。
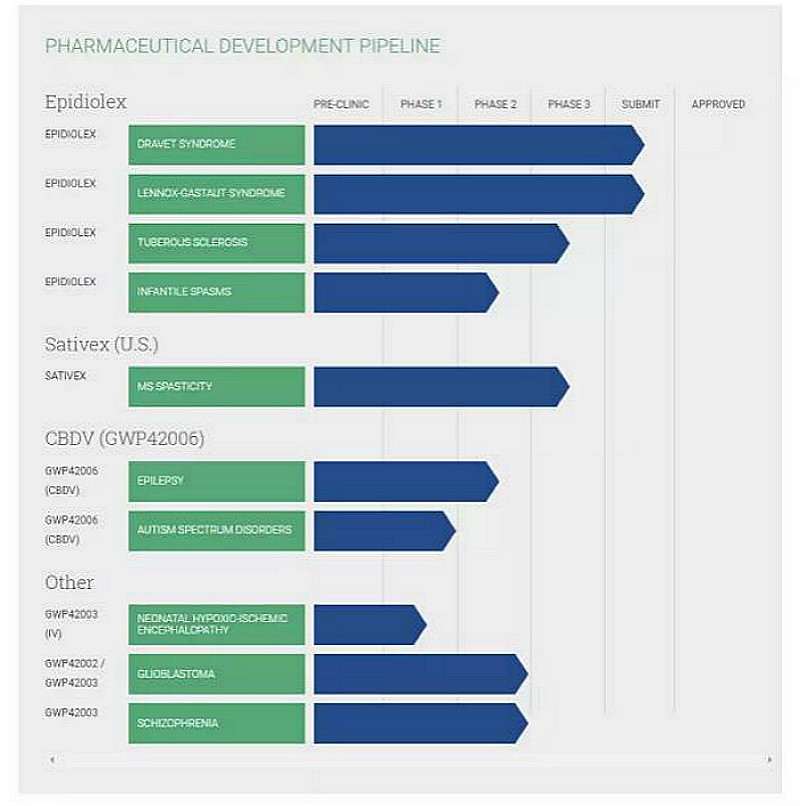
▲GW Pharmaceuticals公司研发管线(图片来源:GW Pharmaceuticals官方网站)
主要研究者之一、麻省总医院儿科癫痫主任兼哈佛大学医学院神经病学教授Elizabeth Thiele博士说:“按照现有的情况看,患者及其家属通常难以控制癫痫发作,而研究表明,这种CBD药物制剂可能提供新的治疗方案,这对某些患者可能有效。”
“我们很高兴咨询委员会一致建议批准Epidiolex,这将为LGS和Dravet综合征患者提供重要的治疗选择,这是两种最严重和难治性癫痫的形式,”GW首席执行官Justin Gover先生说:“这一有利的结果标志着我们公司坚定不移地致力于解决LGS和Dravet综合征患者未满足需求的重要里程碑,以及我们决心在最高研究和制造标准下研究Epidiolex的决心。我们期待着在Epidiolex的NDA审评过程中与FDA继续进行讨论。”
期待这一药物能在6月顺利得到批准,减少癫痫患者及其家庭的痛苦,尽早过上正常人的生活。
News
相关文章

2023-08-09

2021-09-28
2021-09-28
2021-10-01

2021-10-07
2023-09-07
2021-10-07

2021-10-08

2021-10-09

2021-10-09
Next
下一篇