昨天一位读者私信一度医药,表示“肺动脉高压患者,希望越来越多的新药出现,然后可以进入医保,不然真用不起”。
今天我们就盘点肺动脉高压的医保情况及国内研发现状。
什么是肺动脉高压?
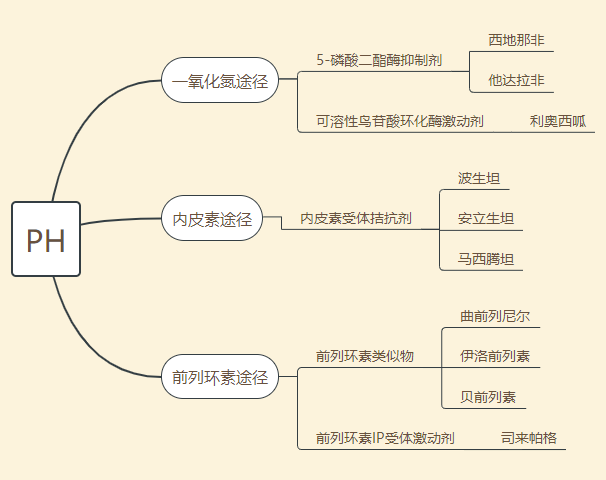
肺动脉高压(pulmonary Artery hypertension,PAH)是常见的肺血管疾病,是多种异源性疾病(病因)和不同发病机制导致肺血管结构或功能改变,引起肺血管阻力和肺动脉压力升高的临床和病理生理综合征,继而发展成右心衰竭甚至死亡。
肺动脉高压非常凶险,一度被称为“心血管疾病中的癌症”,如果不能治疗,患者的平均存活年限仅为2.8年。 我国临床研究表明,中国未经靶向药物治疗者1年生存率仅68%,接受充分靶向治疗后1年生存率可提升至85.4%。
目前,我国肺动脉高压患者保守估计约为500~800万人,但是经过治疗的人非常少,而且其中有90%的患者无法承担高额的医疗费用中断或者放弃治疗。
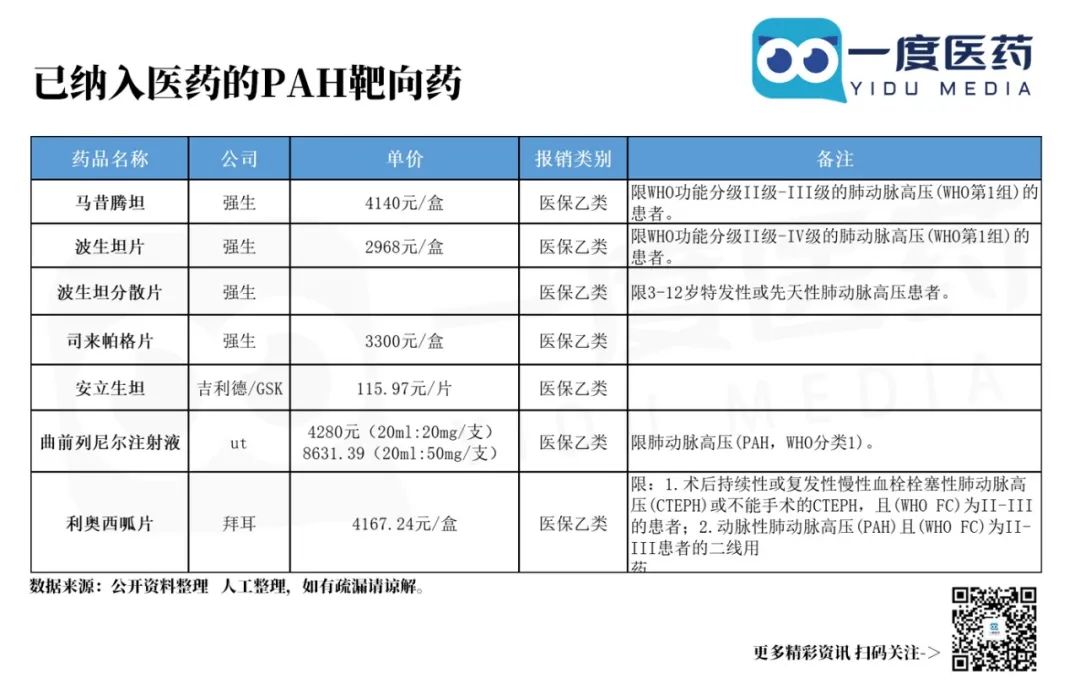
马昔腾坦,8家药企角逐首仿
马昔腾坦是一种内皮素受体拮抗剂(ERA),用于治疗肺动脉高压(PAH,WHO第1组),以延缓疾病进展。其原研企业是瑞士爱可泰隆(Actelion,2017年被强生收购),在2013年10月获得FDA批准上市,商品名为Opsumit。2022年销售额为17.83亿美元,2023年Q1-Q3为14.37亿美元,市场规模较为稳定。
在中国,原研企业爱可泰隆于2016年12月向国家药品监督管理局(NMPA)提交了马昔腾坦片的上市申请,2017年10月获得NMPA批准上市,商品名为傲朴舒。2019年马昔腾坦通过医保谈判被纳入国家医保乙类目录。
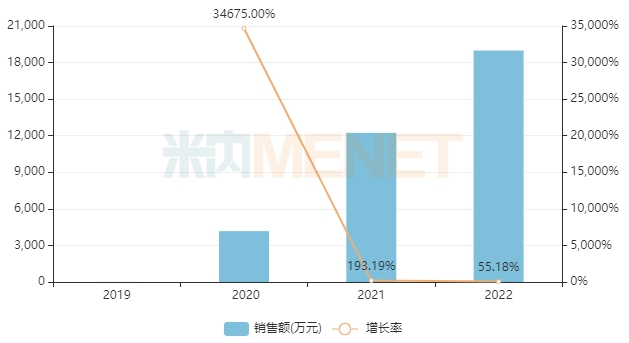
马昔腾坦在国内市场增长迅速,米内网数据显示,2021年马昔腾坦在中国公立医疗机构终端销售额超1.2亿元,同比增长193.19%;2022年销售规模继续稳定扩大,销售额超1.8亿元。
国公立医疗机构终端马昔腾坦片销售情况
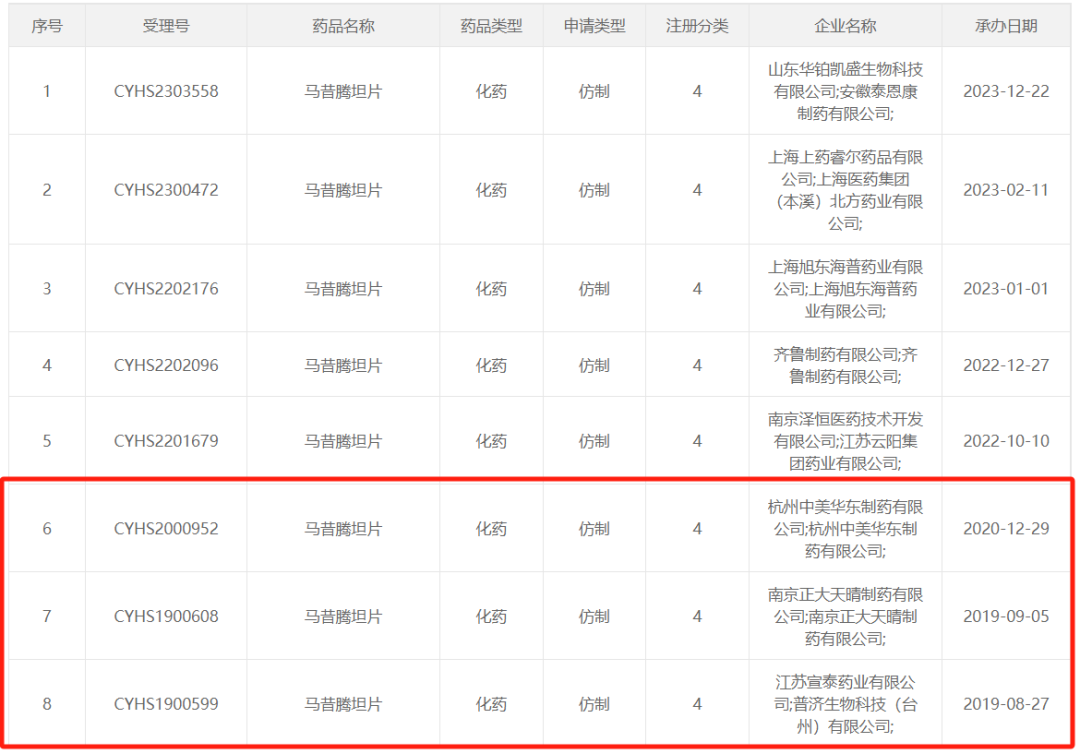
仿制药方面,马昔腾坦的化合物专利CN100432070C已于2021年底到期,其制剂专利CN101262847B将于2026年到期。今年10月份,普济生物、正大天晴和华东医药3家同时拿下马昔腾坦片首仿,另外,泽恒医药、齐鲁制药、海普药业、上药睿尔、华铂凯盛皆相继提交了上市申请,处于审批审批阶段。仿制药上市后,将为患者带来更多的高质量低价格的购药选择。
马昔腾坦仿制药上市申请情况
波生坦,2家药企角逐首仿
波生坦是一种双重内皮素受体拮抗剂,可同时拮抗内皮素A和B受体。研究发现,波生坦可改善肺动脉高压(PAH)患者的临床症状和血流动力学指标,提高运动耐量,生活质量和生存率,推迟临床恶化的时间。
波生坦片原研企业也是瑞士爱可泰隆(Actelion),于2001年11月获得FDA获批上市,用于治疗成人及儿童PAH,商品名为Tracleer,2006年3月国内获批上市。2017年9月,Tracleer分散片被FDA批准用于3岁及以上特发性或先天性PAH患者。
Tracleer是首个获批治疗PAH的药物,专利已于2015年11月过期,销量也随之一落千丈。从2016年的10.35亿美元到2019年3.41亿美元。
在国内,2019年9月在国内获批上市,成为国内首个获批的儿童PAH药物。值得一提的是,Tracleer分散片被列入2019年5月CDE发布的《第二批临床急需境外新药名单》。波生坦片近几年的销售额稳定在1000万元左右,而波生坦分散片作为新品,销售额正逐年上升,2022年销售额约为300万元。
仿制药方面,首访还未诞生,去年迈兰(Mylan) /开心生活、瑞迪博士(Dr. Reddy)依次在国内递交了波生坦片仿制药上市申请。据公开资料,迈兰加拿大子公司Mylan制药的波生坦片于2012年6月获得加拿大卫生部的批准。若顺利,预计迈兰有望取得国内波生坦片首仿资格。
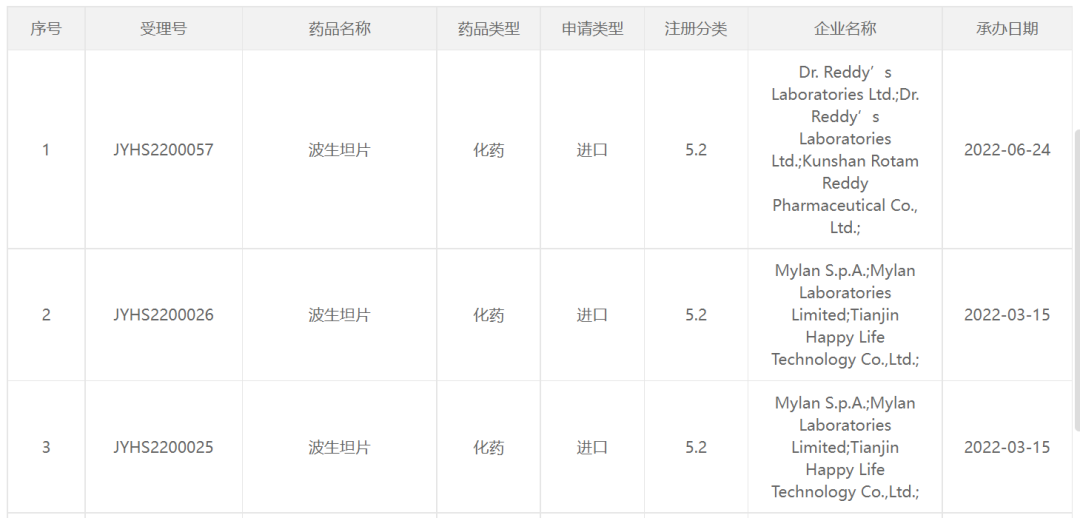
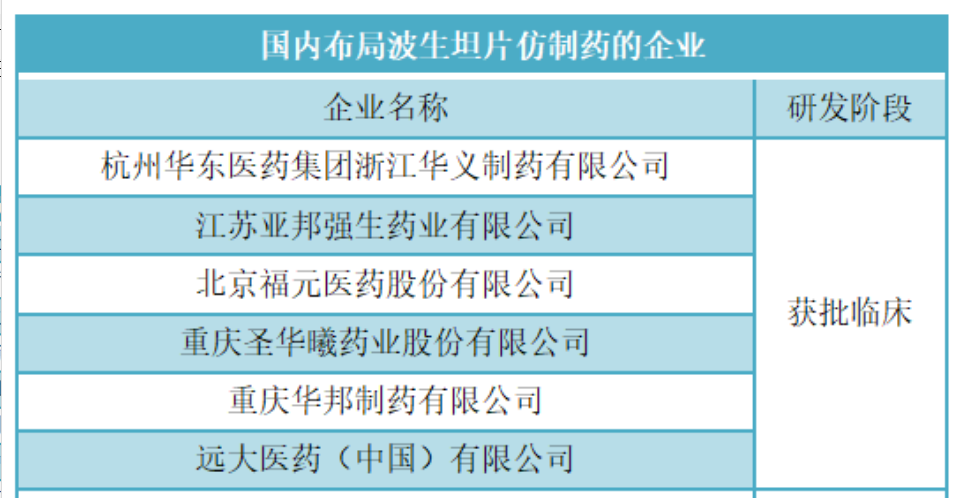
紧随其后的,还有浙江医药股份有限公司新昌制药厂已进入仿制药生物等效性(BE)试验,另外,远大医药、华邦制药、圣华曦药、福元医药、华东医药等皆有布局,且已进入临床阶段。值得一提的是,北京星昊医药股份有限公司还开发了波生坦口崩片,这款2.2类改良型新药已于2021年7月在国内获批临床。
司来帕格片,2家药企角逐首仿
司来帕格片是一种口服有效、高选择性和长效的非前列腺素类前列环素受体(IP受体)激动剂,可改善损伤的肺动脉内皮依赖性舒张,并可能抑制人肺平滑肌细胞的增殖、肺血管壁的增厚,以延缓疾病进展及降低因 PAH 而住院的风险。
司来帕格片原研公司仍是瑞士爱可泰隆(Actelion),2015年12月获得FDA批准,商品名:UPTRAVI。根据强生财报,2027年司来帕格片全球销售额约为5.36亿美元,今年销量稳步增长,2022年全球销量达到13.22亿美元,同比增长6.9%,目前司来帕格片已在全球超过 40 个国家获批。
在我国,该产品同样作为临床急需品种,被纳入优先审评程序加快审评审批,2018年12月获得国家药监局批准批准上市。在国内,根据米内网数据,司来帕格2021年在中国三大终端6大市场的销售额超过1亿元,同比增长263.1%。
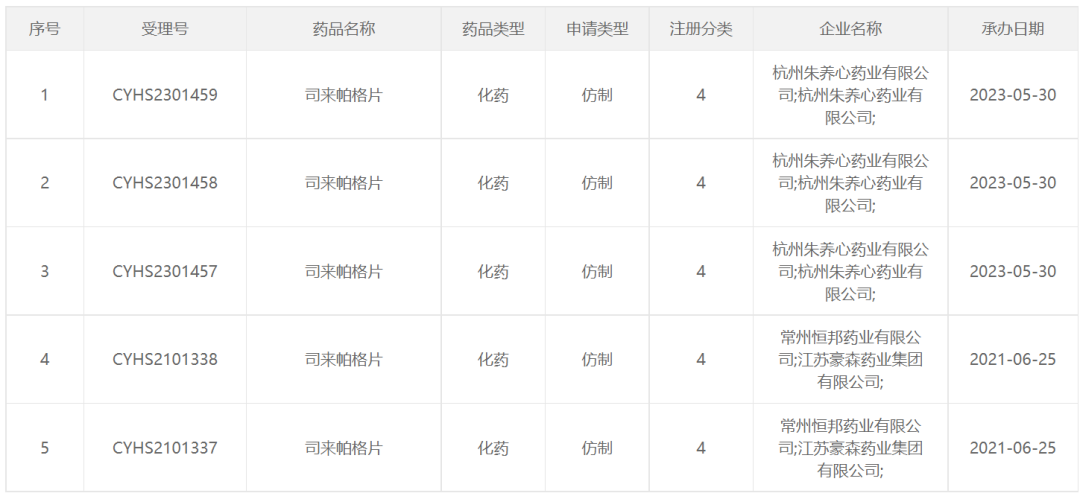
仿制药方面,暂未有司来帕格仿制药获批,并且竞争的企业较少。根据CDE官网查询,目前只有豪森药业、朱养心药业以仿制4类递交了上市申请,豪森药业有望拿下国内首仿。
安立生坦,市场已被国产代替
安立生坦由美国Myogen公司(2006年被吉利德收购获得美国销售所有权,GSK负责美国以外的市场销售权)开发的一种可选择性的内皮素受体拮抗剂(ERA),用以改善运动能力和延缓临床恶化。于2007年6月获得FDA批准上市,用于治疗有WHOⅡ级或Ⅲ级症状的肺动脉高压患者(WHO组1),商品名为“Letairis”。2015年11月专利到期,受到仿制药的影响,安立生坦销售额一路下跌,从2014年的9.09亿美元,降到2018年4.6亿美元。
在我国,该产品于2010年批准上市。从2019到2021年,安立生坦片全国样本医院销量翻了26倍,中国更多的PAH患者得到治疗。同时集采的加入对国内市场重新洗牌,只有华海药业和恒邦药业中选,华海药业销售额增长了21%,恒邦药业增长了19%,占据市场份额最大,达到46%。与此相对,吉利德/GSK的安立生坦片未中选,市场份额从65%下降至11%,跌幅明显。

曲前列尼尔,已有2家药企仿制药获批上市
曲前列尼尔是前列环素的三环联苯胺类似物,通过直接舒张肺和全身动脉血管床,抑制血小板聚集和平滑肌细胞增生而发挥治疗作用。其原研企业为美国United Therapeutics Corporation(简称:ut),于2001年获得FDA优先审批批准上市,商品名为:Remodulin,批准规格为1mg/ml、2.5mg/ml、5mg/ml、10mg/ml。曲前列尼尔半衰期长、药物结构稳定、使用方便,作为一线治疗和抢救药物应用广泛。先后已在欧洲、日本等超过30个国家上市。根据IMS数据,曲前列尼尔2020年全球市场的销售额约5.17亿美元。
2010年7月李氏大药厂和美国United Therapeutics签订了曲前列尼尔注射液在大中华区的独家权利,并将产品引进中国,2011年8月李氏通过兆科合肥向当时的CFDA提交免除临床试验直接上市的申请,2013年获得上市批准,当时标价高达9.99万/支,一个疗程需要四支。
仿制药方面,今年3月,众强药业刚获得曲前列尼尔注射液上市批准,江苏众强药业是国产第二家,为第一家是兆科药业。
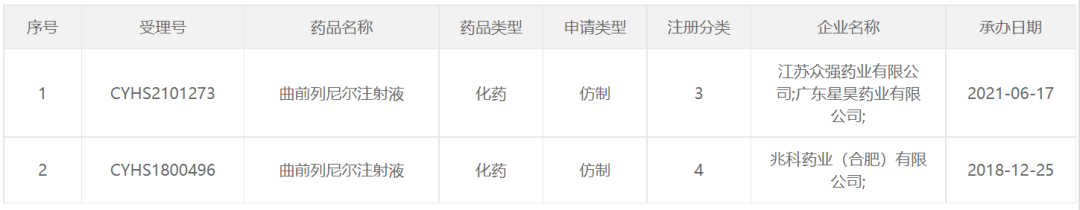
2021年3月,复星医药与江苏众强药业有限公司达成合作,复星医药引进曲前列尼尔(商品名:润漠德霖)并获独家商业化权利。销售方面,根据米内网数据,曲前列尼尔注射液近年来在中国公立医疗机构终端销售额增速惊人,2021年同比增长186.89%。
News
相关文章

2021-10-09

2021-10-08

2021-10-07

2021-10-14
2021-10-16

2021-10-16

2021-10-19

2021-10-19

2021-10-20

2021-10-20
Next
下一篇