文 | winter
12 月 27 日,强生的 Guselkumab 注射液(受理号:JXSS1900035)获国家药监局批准上市,该品种是全球第一个上市的只针对 IL-23 的单抗药物,用于治疗成人中重度斑块状银屑病。
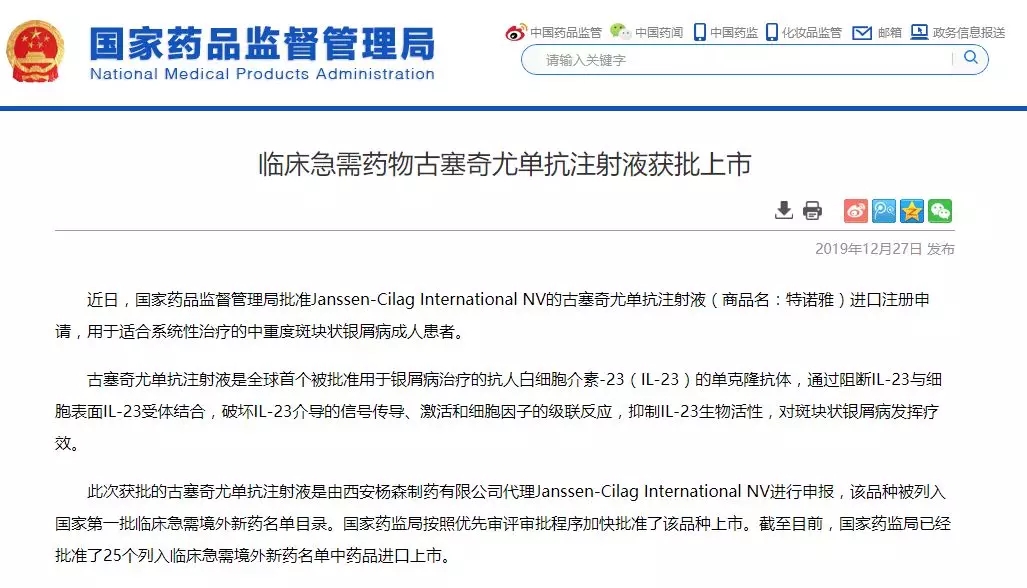
Guselkumab(商品名:Tremfya,中文名商品名:特诺雅)是一款可以与白细胞介素-23(IL-23) 的 p19 亚基结合,阻断 IL-23 作用的人源化单克隆抗体。2017 年 7 月 FDA 批准 Tremfya 治疗中重度斑块状银屑病。2019 年 2 月获 FDA 批准自行注射版(One-Press Patient-Controlled Injector)用于治疗成人斑块状银屑病。
2017 年 7 月 13 日,Guselkumab(商品名:Tremfya)获 FDA 批准,用于治疗中至重度斑块状银屑病。截至目前,Tremfya 已在全球多个国家和地区获得批准,用于中度至重度斑块型银屑病成人患者的治疗。
根据强生财报显示,2018 年全球销售额达到 5.44 亿美元,2019 年前三季度 Tremfya 累计销售额达到 7.42 亿美元。根据 EvaluatePharma 预测,Tremfya 到 2023 年销售额将突破 30 亿美元。
在中国,Tremfya(特诺雅)于 2018 年 11 月在香港获批上市,2019 年 6 月 22 日在国家药监局申报上市。早在 2018 年 Tremfya 就被列入国家《第一批临床急需境外新药名单》,治疗适应症为:红皮型银屑病、斑块型银屑病、脓疱型银屑病、银屑病关节炎、寻常型银屑病。
临床数据显示,Guselkumab 在和阿达木单抗头对头治疗银屑病患者的 III 期临床中,取得了优效性结果,主要终点 16 周时的 PASI 90 为 73% vs. 41%。
此外,强生于今年 8 月公布了 guselkumab vs. secukinumab 用于治疗中重度斑块型银屑病的头对头 III 期 ECLIPSE 研究的结果,在主要终点(48 周时 PASI 90)上,guselkumab 优于 secukinumab(84.5% vs. 70%),达到了临床上的显著(P<0.001)。在次要终点上,包括 12 周和 48 周时 PASI 75 以及 48 周时 PASI 100,两者的疗效相近。
News
相关文章
2023-09-07

2021-10-07

2021-10-08

2021-10-14

2021-10-15
2021-10-19

2021-10-20

2021-10-22
2021-10-22
2021-10-22
Next
下一篇